Termodinamik, ısı ve diğer enerji biçimleri arasındaki ilişkilerle ilgilenen fizik dalıdır. Özellikle, termal enerjinin diğer enerji formlarına nasıl dönüştürüldüğünü ve termal enerjinin maddeyi nasıl etkilediğini açıklar.
Termal enerji, bir maddenin veya sistemin sıcaklığından dolayı sahip olduğu enerjidir. Başka bir deyişle, Kentucky Üniversitesi’ne göre hareket eden veya titreyen moleküllerin enerjisidir. Missouri Southern State Üniversitesi’nde fizik profesörü olan David McKee, verdiği demeçte, termodinamik, “aşırı derecede karmaşık” olabilen bu enerjiyi ölçmeyi içerir.

“Termodinamikte incelediğimiz sistemler çok büyük sayıda atomdan oluşur, veya karmaşık yollarla etkileşime giren moleküller. Ancak bu sistemler denge dediğimiz doğru kriterleri sağlıyorsa çok az sayıda ölçüm veya sayı ile tanımlanabilirler. Genellikle bu, sistemin kütlesi, sistemin basıncı ve sistemin hacmi veya başka bir eşdeğer sayı kümesi olarak idealleştirilir.”
Sıcaklık

O halde termodinamik, maddenin çeşitli özellikleriyle ilgilenir; Bunların başında ısı gelir. Georgia Eyalet Üniversitesi’ne göre ısı, aralarındaki sıcaklık farkı nedeniyle maddeler veya sistemler arasında aktarılan enerjidir. Bir enerji biçimi olarak ısı korunur – yaratılamaz veya yok edilemez. Ancak bir yerden başka bir yere aktarılabilir.
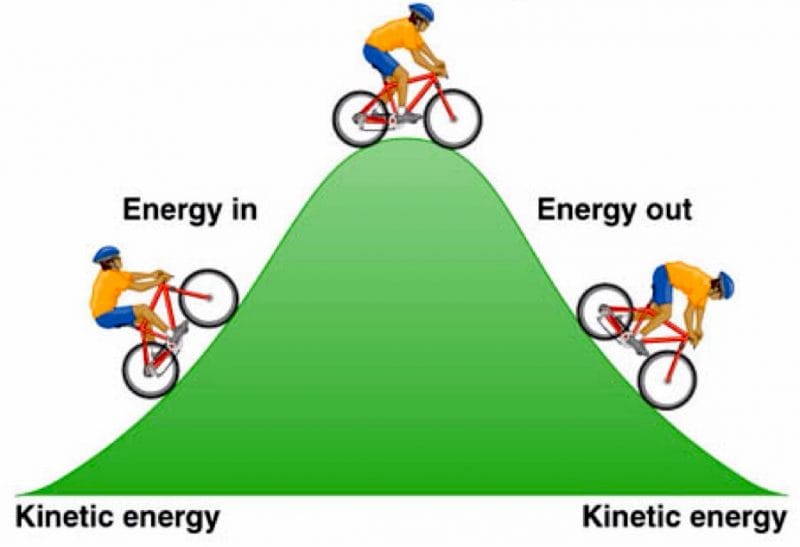
Isı ayrıca diğer enerji formlarına dönüştürülebilir. Örneğin, bir buhar türbini, kinetik enerjiyi elektrik enerjisine dönüştüren bir jeneratörü çalıştırmak için ısıyı kinetik enerjiye dönüştürebilir. Bir ampul, bu elektrik enerjisini, bir yüzey tarafından emildiğinde tekrar ısıya dönüştürülen elektromanyetik radyasyona (ışık) dönüştürebilir. Bu süreç boyunca, enerjinin bir kısmı entropiye dönüşür.
Georgia State Üniversitesi’ne göre, bir madde tarafından aktarılan ısı miktarı, hareket halindeki o maddenin atomlarının veya moleküllerinin hızına ve sayısına bağlıdır. Atomlar veya moleküller ne kadar hızlı hareket ederse, sıcaklık o kadar yüksek olur ve hareket halindeki atomlar veya moleküller ne kadar fazlaysa, aktardıkları ısı miktarı o kadar büyük olur.
American Heritage Dictionary’e göre sıcaklık, “standart bir ölçekte belirlenmiş birimler veya dereceler cinsinden ifade edilen, bir madde örneğindeki parçacıkların ortalama kinetik enerjisinin bir ölçüsüdür”. En yaygın olarak kullanılan sıcaklık ölçeği, suyun donma ve kaynama noktalarını temel alan ve sırasıyla 0 C ve 100 C değerlerini atayan Celsius’tur. Fahrenheit ölçeği ayrıca, atanmış değerlere sahip suyun donma ve kaynama noktalarına da dayanır. Sırasıyla 32 derece Fahrenheit ve 212 F.
Bununla birlikte, dünya çapındaki bilim adamları, İskoçya Ulusal Kütüphanesine göre, suyun donma ve kaynama noktalarından ziyade toplam termal enerjiye dayandığından, William Thomson, 1. . Bu ölçek, Celsius ölçeğiyle aynı artışları kullanır; örneğin, 1 C’lik bir sıcaklık değişimi 1 K’ye eşittir. Bununla birlikte, Kelvin ölçeği mutlak sıfırda, yani toplam ısı enerjisinin bulunmadığı sıcaklıkta başlar ve tüm moleküler hareket durur. 0 K sıcaklık eksi 459.67 F veya eksi 273.15 C’ye eşittir.
Özısı
Wolfram Research’e göre, bir maddenin belirli bir kütlesinin sıcaklığını belirli bir miktarda artırmak için gereken ısı miktarına özgül ısı veya özgül ısı kapasitesi denir . Bunun için geleneksel birim Kelvin başına gram başına kaloridir. Kalori, 1 gram suyun sıcaklığını 4 C’de 1 derece yükseltmek için gereken ısı enerjisi miktarı olarak tanımlanır.
Bir metalin özgül ısısı, numunenin kütlesine değil, neredeyse tamamen numunedeki atom sayısına ve bunların bağlanma şekline bağlıdır. Örneğin, bir kilogram alüminyum , bir kilogram kurşundan yaklaşık yedi kat daha fazla ısı emebilir . Bununla birlikte, Güneydoğu Louisiana Üniversitesi’ne göre, belirli bir su kütlesi, su moleküllerini bağlayan güçlü kuvvetler sayesinde, eşit bir alüminyum kütlesinden yaklaşık beş kat daha fazla ısı emebilir .
Termal İletkenlik

Termal iletkenlik ( k ), Debdatta Ratna’nın “Thermosets” adlı kitabına göre (Woodhead Publishing limited, 2012) “belirli bir malzemenin belirli bir kesitinden ısının geçme hızı”dır. Swarthmore College’a göre k birimi, Kelvin (K) başına metre (m) başına watt (W)’dir . Bakır ve gümüş gibi metaller için k değerleri sırasıyla 380 ve 420 W/m·K’de nispeten yüksektir.
Bu özellik, bu malzemeleri otomobil radyatörleri ve bilgisayar çipleri için soğutma kanatçıkları için kullanışlı hale getirir, çünkü bunlar ısıyı hızlı bir şekilde taşıyıp çevre ile değiş tokuş edebilirler. K’nin en yüksek değeri Materials dergisinde yayınlanan 2009 tarihli bir araştırmaya göre, herhangi bir doğal madde için 2.200 W/m·K değerinde elmas bulunur .
Diğer malzemeler, son derece zayıf ısı iletkenleri oldukları için yararlıdır; bu özellik, ısıl direnç veya ısının malzeme yoluyla iletilme hızını tanımlayan R değeri olarak adlandırılır. Fiberglas, kaz tüyü ve strafor gibi bu malzemeler, dış cephe duvarlarında, kışlık mantolarda ve termal kahve kupalarında yalıtım için kullanılmaktadır. Açık kaynaklı bir ders kitabı olan OpenStax’a göre R değeri, İngiliz ısı birimi (ft2·°F·h/Btu) başına fit kare çarpı derece Fahrenheit çarpı saat cinsinden verilir.
Newton’un Soğutma Yasası
1701’de Sir Isaac Newton , Royal Society’nin Felsefi İşlemlerinde “Scala graduum Caloris” (“Isı Derecelerinin Bir Ölçeği”) başlıklı kısa bir makalede Soğutma Yasasını ilk kez dile getirdi . Newton’un yasayla ilgili ifadesi, orijinal Latince’den “ısı derecelerinin fazlalığı … zamanlar aritmetik bir ilerlemedeyken geometrik ilerlemedeydi” olarak tercüme edilir.
Worcester Polytechnic Institute, bu bilimsel yasanın daha modern bir versiyonunu “sıcaklığın değişim hızı, nesnenin sıcaklığı ile çevreleyen ortamın sıcaklığı arasındaki farkla orantılıdır” şeklinde verir.
Bu , sıcaklık farkında üstel bir azalmaya neden olur. Örneğin, soğuk bir banyoya ılık bir cisim konursa, belirli bir süre içinde iki sıcaklık arasındaki fark yarı yarıya azalacaktır. Daha sonra aynı süre içinde kalan fark yine yarı yarıya azalacaktır. Sıcaklık farkının bu tekrarlanan yarıya bölünmesi, ölçülemeyecek kadar küçük olana kadar eşit zaman aralıklarında devam edecektir. Bu noktada, sistem termal dengededir.
Isı Transferi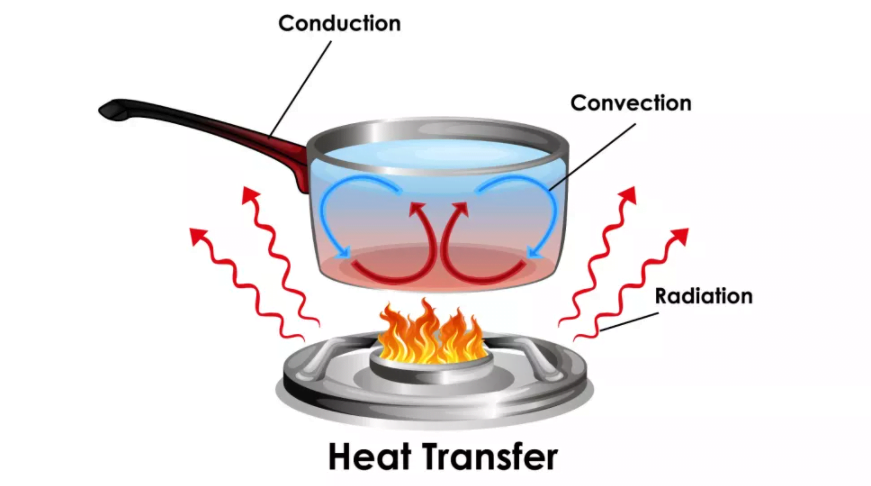
Isı transferinin nasıl çalıştığını gösteren diyagram.(Resim kredisi: Getty Images aracılığıyla blueringmedia)Isı, bir vücuttan diğerine veya bir vücut ile çevre arasında üç farklı yolla aktarılabilir: iletim, taşınım ve radyasyon. İletim, enerjinin katı bir maddeden aktarılmasıdır. Cisimler arasındaki iletim, doğrudan temas halinde olduklarında meydana gelir ve moleküller enerjilerini arayüz boyunca aktarır.
Konveksiyon, ısının akışkan bir ortama veya ortamdan aktarılmasıdır. Katı bir cisimle temas halindeki bir gaz veya sıvıdaki moleküller, o cisimden veya cisme ısı iletir veya emer ve sonra uzaklaşarak sıvının diğer moleküllerinin yerlerine hareket etmesine ve işlemi tekrarlamasına izin verir.
Radyasyon, elektromanyetik (EM) radyasyon , özellikle ısı enerjisi taşıyan kızılötesi fotonlar yoluyla enerji emisyonudur. Northwestern Üniversitesi’ne göre, tüm maddeler bir miktar EM radyasyonu yayar ve emer; bunun net miktarı, bunun ısıda bir kayıp veya artışa neden olup olmadığını belirler .
Carnot Döngüsü
1824’te Nicolas Léonard Sadi Carnot , Amerikan Makine Mühendisleri Derneği’ne göre, Carnot çevrimi olarak bilinen şeye dayanan bir ısı motoru için bir model önerdi. Döngü, gazların basıncı, hacmi ve sıcaklığı arasındaki ilişkilerin yanı sıra bir enerji girişinin nasıl biçim değiştirebileceğini ve sistem dışında nasıl iş yapabileceğini kullanır.
Carnot çevrimindeki ilk adım, izotermal genleşmedir, burada bir pistondan gelen basınç altında bir silindirdeki gaz sabit bir sıcaklıkta tutulur, ancak bir ısı kaynağı silindirle temas ettirilir. Aynı sıcaklığı korumak için gazın genleşmesi gerekir. Daha sonra, adyabatik genişleme veya çevreye ısı transferi olmadan genişleme, gazın daha fazla genişlemesine izin vermek için pistondan ağırlığı kaldırır, bu da iş yapmak için bir silindiri itmesine yardımcı olur. (Adyabatik, termodinamikte çalışma akışkanında ısı ve kütle kaybının veya kazancının olmadığı haldeki süreçtir.)
Daha sonra, gaz sabit bir sıcaklıkta soğutulur ve gazdaki basıncı yükseltmek için pistona ağırlık eklenerek sıkıştırılır, bu noktada ısı gazdan ısı kaynağına geri döner. Son olarak, adyabatik sıkıştırma, gazın basıncını daha da artırmak ve dolayısıyla sıcaklığını artırmak için pistona daha fazla ağırlık ekler. Daha sonra döngü, duruma göre tekrarlanır. NASA’ya. Georgia Eyalet Üniversitesi’ne göre ısıtma, iklimlendirme ve soğutma için kullanılan ısı pompalarının arkasındaki temel ilke budur .
Termodinamik ve Entropi

Tüm termodinamik sistemler atık ısı üretir. Bu atık, bir sistemin düzensizliğinin bir ölçüsü olan entropide bir artışa neden olur. İş, düzenli moleküler hareketten geldiğinden, Britannica’ya göre entropi, iş yapmak için mevcut olmayan enerjinin bir ölçüsüdür . Herhangi bir kapalı sistemde entropi her zaman artar; asla azalmaz . Ek olarak, hareketli parçalar sürtünme nedeniyle atık ısı üretir ve sistemden ışıma ısısı kaçınılmaz olarak sızar.
Bu, sözde sürekli hareket makinelerini imkansız hale getirir. Missouri Eyalet Üniversitesi’nde fizik profesörü olan Siabal Mitra, şunları söyledi: “% 100 verimli bir motor yapamazsınız, bu da sürekli bir hareket makinesi yapamazsınız anlamına gelir. Ancak, dışarıda hala yapmayan birçok insan var. Buna inanmayın ve hala sürekli hareket eden makineler yapmaya çalışan insanlar var.”
Entropi aynı zamanda “kapalı bir sistemdeki düzensizliğin veya rastgeleliğin bir ölçüsü” olarak da tanımlanır ve bu da kaçınılmaz olarak artar. Sıcak ve soğuk suyu karıştırabilirsiniz, ancak büyük bir bardak ılık su, sıcak ve soğuk su içeren iki küçük bardaktan daha düzensiz olduğundan, sisteme enerji eklemeden asla tekrar sıcak ve soğuk olarak ayıramazsınız. Başka bir deyişle, bir yumurtayı çözemez veya kahvenizden krema çıkaramazsınız. Bu nedenle entropi bize bir zaman oku sağlar: ileri, artan entropinin yönüdür.
Termodinamik Yasaları

Termodinamiğin temel ilkeleri başlangıçta üç yasada ifade edildi. Daha sonra bilim adamları, daha temel bir yasanın, açıkça belirtilmesine gerek kalmayacak kadar açık göründüğü için ihmal edildiğini anladılar. Eksiksiz bir kurallar dizisi oluşturmak için bilim adamları, bu en temel yasanın dahil edilmesi gerektiğine karar verdiler. Ancak sorun, ilk üç yasanın zaten kurulmuş olması ve atanan numaralarıyla iyi bilinmesiydi.
Önemli bir kafa karışıklığına yol açabilecek mevcut yasaları yeniden numaralandırma ya da en önemli yasayı listenin sonuna koyma olasılığıyla karşı karşıya kaldığında, ki bu hiçbir mantıklı anlam ifade etmeyecekti, İngiliz fizikçi Ralph H. Fowler, ikilemi çözdü: yeni yasaya “Sıfırıncı Yasa” adını verdi.
Termodinamik yasaları kaç tanedir?
İşte kısaca, dört termodinamik yasası:
Termodinamiğin Sıfırıncı Yasası, iki cisim üçüncü bir cisimle termal dengedeyse, o zaman birbirleriyle de dengede olduklarını belirtir. Bu, sıcaklığı maddenin temel ve ölçülebilir bir özelliği olarak belirler.
Termodinamiğin Birinci Yasası, bir sistemin enerjisindeki toplam artışın, termal enerjideki artış ile sistem üzerinde yapılan işin toplamına eşit olduğunu belirtir. Bu, ısının bir enerji biçimi olduğunu ve bu nedenle korunum ilkesine tabi olduğunu belirtir – yani ne yaratılabilir ne de yok edilebilir.
Termodinamiğin İkinci Yasası, ısı enerjisinin daha düşük sıcaklıktaki bir vücuttan daha yüksek sıcaklıktaki bir vücuda enerji ilavesi olmadan aktarılamayacağını belirtir. Bu nedenle bir klimayı çalıştırmak için para harcamak gerekir.
Termodinamiğin Üçüncü Yasası, mükemmel bir kristalin – yani mükemmel bir şekilde düzenlenmiş, simetrik bir modelde düzenlenmiş atomlardan oluşan bir maddenin – mutlak sıfırda entropisinin sıfır olduğunu belirtir.
Yukarıda açıklandığı gibi, entropi bazen “atık enerji” veya iş yapamayan enerji olarak adlandırılır; ve mutlak sıfırda herhangi bir ısı enerjisi olmadığından, atık enerji de olamaz. Entropi aynı zamanda bir sistemdeki düzensizliğin bir ölçüsüdür ve mükemmel bir kristal tanım gereği mükemmel bir şekilde düzenlenmiş olsa da, herhangi bir pozitif sıcaklık değeri, kristal içinde düzensizliğe neden olan hareket olduğu anlamına gelir. Bu nedenlerle, daha düşük entropili fiziksel bir sistem olamaz, bu nedenle entropi her zaman pozitif bir değere sahiptir.
Termodinamik bilimi yüzyıllar boyunca gelişmiştir ve ilkeleri şimdiye kadar icat edilen hemen hemen her cihaz için geçerlidir. Modern teknolojideki önemi göz ardı edilemez.
Nimet Kılıç